Температура открытого пламени и огня в зажигалке
Содержание:
Температура пламени
 Для разных горючих паров и газов температура пламени неодинакова. А ещё неодинакова температура разных частей пламени, а область полного сгорания имеет более высокие показатели температуры.
Для разных горючих паров и газов температура пламени неодинакова. А ещё неодинакова температура разных частей пламени, а область полного сгорания имеет более высокие показатели температуры.
Некоторое количество горючего вещества при сжигании выделяет определённое количество теплоты. Если строение вещества известно, то можно рассчитать объём и состав полученных продуктов горения. А если знать удельную теплоту этих веществ, то можно рассчитать ту максимальную температуру, которую достигнет пламя.
Стоит помнить о том, что если вещество горит в воздухе, то на каждый объём вступающего в реакцию кислорода приходится четыре объёма инертного азота. А так как в пламени присутствует азот, он нагревается теплотой, которая выделяется при реакции. Исходя из этого можно сделать вывод о том, что температура пламени будет состоять из температуры продуктов горения и азота.
Невозможно точно определить температуру, но можно это сделать приблизительно, так как удельная теплота изменяется с температурой.
Вот некоторые показатели по температуре открытого огня в разных материалах.
- Горение магния — 2200 градусов.
- Горение спирта не превышает температуры 900 градусов.
- Горение бензина — 1300−1400 градусов.
- Керосина — 800, а в среде чистого кислорода — 2000 градусов.
- Горение пропан-бутана может достигать температуры от 800 до 1970 градусов.
- При сгорании дерева температурный показатель колеблется от 800 до 1000 градусов, а воспламеняется оно при 300 градусах.
- Температурный параметр горения спички составляет 750−850 градусов.
- В горящей сигарете — от 700 до 800 градусов.
- Большинство твёрдых материалов воспламеняется при температурном показателе в 300 градусов.
Процесс горения газа
Категория: Газоснабжение
Процесс горения газа
Основным условием для горения газа является наличие кислорода (а следовательно, воздуха). Без присутствия воздуха горение газа невозможно. В процессе горения газа происходит химическая реакция соединения кислорода воздуха с углеродом и водородом топлива. Реакция происходит с выделением тепла, света, а также углекислого газа и водяных паров.
В зависимости от количества воздуха, участвующего в процессе горения газа, происходит полное или неполное его сгорание.
При достаточном поступлении воздуха происходит полное сгорание газа, в результате которого продукты его горения содержат негорючие газы: углекислый газ С02, азот N2, водяные пары Н20. Больше всего (по объему) в продуктах горения азота — 69,3—74%.
Для полного сгорания газа также необходимо, чтобы он смешивался с воздухом в определенных (для каждого газа) количествах. Чем выше калорийность газа, тем требуется большее количество воздуха. Так, для сжигания 1 м3 природного газа требуется около 10 м3 воздуха, искусственного — около 5 м3, смешанного — около 8,5 м3.
При недостаточном поступлении воздуха происходит неполное сгорание газа или химический недожог горючих составных частей; в продуктах сгорания появляются горючие газы—окись углерода СО, метан СН4 и водород Н2
При неполном сгорании газа наблюдается длинный, коптящий, светящийся, непрозрачный, желтого цвета факел.
Таким образом, недостаток воздуха приводит к неполному сгоранию газа, а избыток — к чрезмерному охлаждению температуры пламени. Температура воспламенения природного газа 530 °С, коксового — 640 °С, смешанного — 600 °С. Кроме того, при значительном избытке воздуха также происходит неполное сгорание газа. При этом наблюдается конец факела желтоватого цвета, не вполне прозрачный, с расплывчатым голубовато-зеленым ядром; пламя неустойчиво и отрывается от горелки.
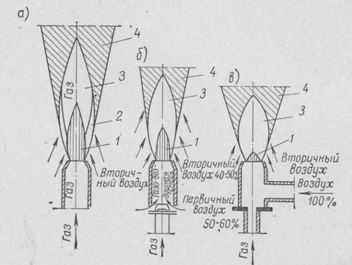
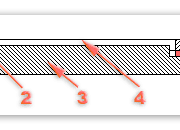
Рис. 1. Пламя газа я — без предварительного смешения газа с воздухом; б —с частичным пред. верительным смешением газа с воздухом; в — с предварительным полным смешением газа с воздухом; 1 — внутренняя темная зона; 2 — коптящий светящийся конус; 3 — горящий слой; 4 — продукты сгорания
В первом случае (рис. 1,а) факел имеет большую длину и состоит из трех зон. В атмосферном воздухе горит чистый газ. В первой внутренней темной зоне газ не горит: он не смешан с кислородом воздуха и не нагрет до температуры воспламенения. Во вторую зону воздух поступает в недостаточном количестве: его задерживает горящий слой, и поэтому он не может хорошо смешаться с газом. Об этом свидетельствует ярко светящийся, светло-желтый коптящий цвет пламени. В третью зону воздух поступает в достаточном количестве, кислород которого хорошо смешивается с газом, газ горит голубоватым цветом.
При этом способе газ и воздух подаются в топку раздельно. В топке происходит не только сжигание газовоздушной смеси, но и процесс приготовления смеси. Такой метод сжигания газа широко применяют в промышленных установках.
Во втором случае (рис. 1,6) сжигание газа происходит значительно лучше. В результате частичного предварительного смешивания газа с воздухом в зону горения поступает приготовленная газовоздушная смесь. Пламя становится короче, несветящимся, имеет две зоны — внутреннюю и наружную.
Газовоздушная смесь во внутренней зоне не горит, так как она не нагревалась до температуры воспламенения. В наружной зоне сгорает газовоздушная смесь, при этом в верхней части зоны резко повышается температура.
При частичном смешении газа с воздухом в этом случае полное сгорание газа происходит только при дополнительном подводе воздуха к факелу. В процессе горения газа воздух подводят дважды: первый раз — до поступления в топку (первичный воздух), второй раз — непосредственно в топку (вторичный воздух). Этот метод сжигания газа положен в основу устройства газовых горелок для бытовых приборов и отопительных котельных.
В третьем случае факел значительно укорачивается и газ сгорает полнее, так как газовоздушная смесь была предварительно приготовлена. О полноте сгорания газа свидетельствует короткий прозрачный факел голубого цвета (беспламенное горение), которое применяют в приборах инфракрасного излучения при газовом отоплении.
Воспламенение — метан
Воспламенения метана происходят не только тогда, когда взрывание зарядов осуществляют в заранее загазовавшейся среде.
Реакция воспламенения метана может сенсибилизироваться или инги-бироваться различными веществами. Так, Одибер показал, что контакт с твердой поверхностью некоторых веществ является важнейшим фактором возникновения воспламенения метано-воздушной смеси. Температура, при которой происходит воспламенение метано-воздушной смеси, может быть резко снижена — вплоть до комнатной — присутствием малых количеств газов или паров.
Температура воспламенения метана на воздухе очень высокая ( выше 600) и мало изменяется в зависимости от условий. Смеси метана с воздухом, содержащие от 5 до 15 об. % метана, взрываются. Особенно велика опасность взрывов метана в угольных шахтах.
|
Катализаторы и ингибиторы горения водороде — и углеводорода-кислородных смесей. |
Наиболее эффективными ингибиторами воспламенения метана оказа — лись органические соли щелочных металлов ароматического ряда, которые можно назвать катализаторами-ингибиторами, поскольку органическая часть молекулы этих добавок может связывать промежуточные активные продукты в менее активные, не способные продолжать цепь окисления и тем самым также ингибировать процесс.
Созданные таким способом водяные завесы предотвращают воспламенение метана в забое выработки.
Определение возможности примене-ння фреонов для предотвращения воспламенения метана.
В работе сделана попытка разделить ингибиторы воспламенения метана на термические и химические; предполагается, что первые действуют благодаря охлаждению пламени, а на поверхности вторых происходит рекомбинация радикалов -, распространяющих цепь реакции.
Как видно из этой таблицы, температура воспламенения метана выше, чем у других горючих газов. Это объясняется прочной структурой его молекулы и межатомных связей в последней, при которых для возникновения цепной реакции горения необходимо высокое значение энергии активации. Температура воспламенения смесей гомологов метана с воздухом понижается по мере увеличения числа углеродных атомов в молекуле.
|
Изменение пределов воспламенения метана от величины пламени и продолжительности контакта.| Изменение пределов. |
На рис. 51 показано влияние на пределы воспламенения метана примеси азота и других негорючих газов. Область воспламенения сокращается, и при определенной концентрации негорючих газов смесь перестает воспламеняться.
Для установления механизма химического действия изученного типа ингибиторов воспламенения метана ( впрочем, это относится и к ингибиторам, описанным в литературе) необходимо провести анализ продуктов горения метана.
Исходя из представлений, изложенных выше, наиболее эффективными ингибиторами воспламенения метана должны быть, по-видимому, органические соли щелочных металлов, главным образом ароматические.
|
Кинетические кривые окисления этана ( по Садовяинову. |
Аналогичные выводы были сделаны позднее Гарнером при изучении окисления и воспламенения метана. Как пишет автор, основной реакцией, идущей в пламени метана, является окисление окиси углерода, и что поэтому представляется весьма вероятным, что мы имеем здесь дело с воспламенением СО в среде других газов
Процесс — горение — метан
Процесс горения метана состоит из параллельных и последовательных стадий окисления и термического распада. Поэтому экспериментальное и теоретическое исследование процесса в целом представляет значительную трудность.
Процесс горения метана делится на две стадии: 1) быстрое горение во фронте пламени, при котором практически расходуется весь кислород; 2) относительно медленное изменение состава газовой смеси ( Н2О, СО2, СО, Н2, С2Н3 и СН4), протекающее в отсутствии свободного кислорода. Основное количество ацетилена образуется в первой стадии, но образование его продолжается и во второй. Отличительной особенностью процесса термоокислительного пиролиза метана является то, что он сопровождается горением и является огневым процессом. При этом тепло, необходимое для реакции расщепления метана, получается при сжигании части углеводородных газов, поступающих в зону реакции.
Исследования процессов горения метана позволили установить, что образование бенз ( а) пирена может протекать в тех местах топки, где значения коэффициента избытка воздуха ( общее или локальные) меньше 1 и где возможно образование сажи.
Следовательно, в процессе горения метана образуются промежуточные соединения, реакция здесь носит цепной характер.
При температурах около 2000 К определяющей скоростью в процессе горения метана уже является суммарная скорость горения окиси углерода, образовавшейся из метана.
Авторы работы считают, что основные положения, высказанные Семеновым по окислению метана, вполне приемлемы для характеристики процесса горения метана в области высоких температур.
Для этого остывший газ переводят вначале в пипетку, заполненную 33 % — ным КОН, для определения С02, образовавшегося в процессе горения метана, а потом в пипетку, заполненную пирогаллолом, для определения избытка кислорода, не вошедшего в реакцию горения.
Лавров развил дальше теорию стадийного окисления метана и показал, что взаимодействие метана с кислородом протекает по четырем стадиям. Это вытекает из стехиометрии реакции СН4 2О2 СО2 2Н2О, где участвуют четыре атома кислорода и каждый атом способен завершать определенную стадию процесса горения метана.
Исследованиями установлено, что при добавке галоидо-углеводородов концентрация СН радикалов в пламени сильно возрастает. Это объясняется тем, что добавка галоидоуглево-дородов способствует образованию водородообедненных продуктов. Процесс горения метана протекает следующим образом.
|
Тепловой режим горения однопроцентной метано-воздушной смеси. s. |
Пользуясь этим уравнением, рассчитано несколько значений времени пребывания для различных значений средней температуры. Полученные точки нанесены на график ( рис. 3), обобщающий все экспериментальные данные. Хорошее совпадение экспериментальной и теоретической кривых свидетельствует о том, что нуль-размерная схема достаточно точно описывает процесс горения метана в условиях, соответствующих условиям эксперимента и отвечающих процессам в реальных камерах сгорания.
При горении метана, как и при горении углерода твердого топлива, подтверждается закономерность об образовании промежуточного соединения. Таким промежуточным соединением является формальдегид. Антонова, Кузьмин, Мошкина, Налбандян, Нейман, Феклисов , применяя в своей работе кинетический метод меченых атомов, убедительно показали, что при горении метана сначала происходит накопление Н2СО, а после достижения некоторого максимума начинает образовываться окись углерода из формальдегида, таким образом было доказано существование стадии окисления формальдегида до окиси углерода и показано, что СО является первичным окислом углерода при горении метана. Лавров и Петренко показали, что процесс конверсии метана углекислотой и водяными парами также проходит через образование и разрушение формальдегида. В процессе горения метана возникают радикалы СН3 или СН2, которые приводят к образованию формальдегида.
При горении метана, как и при горении углерода твс-рдого топлива, подтверждается закономерность образования промежуточного соединения. Таким промежуточным соединением является формальдегид. Антонова и др., 1955 ], применяя в своей работе кинетический метод меченых атомов, убедительно показали, что при горении метана сначала происходит накопление Н2СО, а после достижения некоторого максимума начинает образовываться СО из формальдегида. Таким образом было доказано существование стадии СН20 — СО и показано, что СО является первичным окислом углерода при горении метана. В процессе горения метана возникают радикалы СН3 или СН2, которые приводят к образованию формальдегида.
Топливо для паяльных ламп
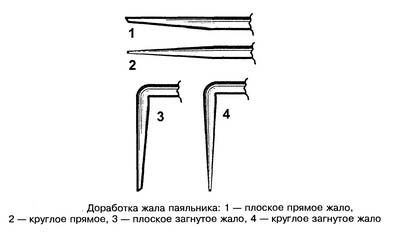
Доработка жала паяльника.
Универсальность паяльной лампы в том, что работать она может практически на любом, способном к возгоранию, жидком топливе: спирте, керосине, бензине, солярке, нефти. Но это вовсе не значит, что в каждую паяльную лампу можно заливать что угодно.
Топливо должно быть качественным. К тому же нужно учитывать, что неподходящий вид топлива очень быстро забьет своими испарениями форсунку. На сегодня паяльные лампы бывают трех видов:
- керосиновые;
- бензиновые;
- спиртовые.
Принцип паяльной лампы сохранился и в работе газовой горелки, поэтому некоторые специализированные источники этот прибор тоже относят к паяльным лампам, выделяя его отдельным, четвертым, видом.
Заправлять лампу другим видом топлива, не соответствующим ее конструкции, категорически запрещается инструкцией по технике безопасности. И это правило должно неукоснительно соблюдаться. Ведь залитый в бензиновую «паялку» керосин сделает из нее инструмент наподобие огнемета. Попадая в горелку, он не успеет полностью испариться, следовательно, гореть будут не пары, а сам керосин. Нормально работать такой инструмент не будет.
Еще опаснее в керосиновую паяльную лампу заливать бензин. Бензин значительно быстрее керосина испаряется, и давление его паров в горелке будет в 6 раз больше расчетного. При попытке зажечь пары взорвутся, превратив полезный инструмент в опасную бомбу. Поэтому, если вы пользуетесь керосиновой паяльной лампой, заправлять ее нужно только чистым керосином, без каких-либо примесей, не используя смесей керосина с бензином или другим топливом.
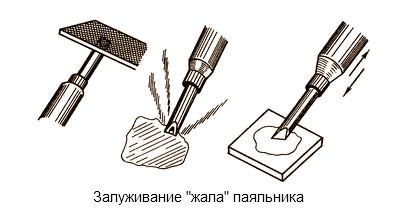
Залуживание жала паяльника.
Та же ситуация и с бензиновой паяльной лампой. Ее нужно заправлять только чистым бензином. При этом показатель октанового числа бензина на работу инструмента практически не оказывает влияния: ни на быстроту воспламенения, ни на время горения, ни на температуру пламени. Но при выборе марки бензина не следует забывать, что у низкооктановых марок различных добавок и примесей намного меньше, поэтому при работе намного меньше будет загрязняться форсунка.
У спиртовых паяльных ламп маленький объем резервуара (всего 200-300 мл), соответственно, ее горение сильно ограничено во времени, поэтому сегодня вместо них мастера предпочитают пользоваться газовыми горелками.
Горение — природный газ
Горение природного газа, как и другого вида топлива, может происходить за счет взаимодействия с атомарным кислородом или гидроксил-ионом.
|
Установка фирмы Сога-bustifium. |
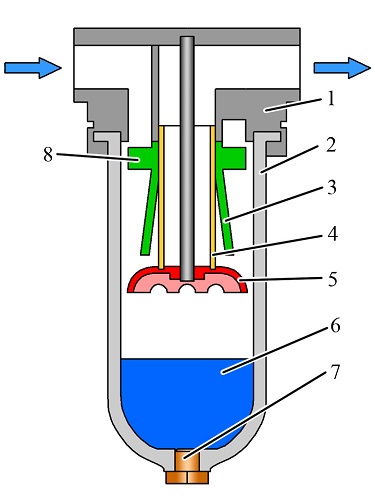
Горение природного газа в смеси с первичным воздухом осуществляется в V-образных полостях 5, имеющих соответствующую перфорацию. Пройдя высокотемпературную зону, вредные органические примеси сгорают и превращаются в безвредные продукты полного сгорания, которые вместе с продуктами сгорания природного газа выбрасываются в атмосферу или поступают в камеру охлаждения котла, сушилки или какого-нибудь другого теплоиспользующего агрегата.
Для горения природного газа в печных установках цементных заводов необходимо практически обеспечить, во-первых, контакт и смешение его с воздухом, во-вторых, начальное и последующее воспламенение непрерывно поступающего газа и, в-третьих, непрерывное и полное сгорание газа.
Продукты горения природного газа отводятся из контактного водонагревателя с температурой 40 С.
Неполнота горения природного газа характеризуется появлением в газах, отходящих из печных и сушильных установок, наряду с углекислотой, азотом и парами воды, также окиси углерода, водорода и метана, а иногда и других углеводородов, продуктов их неполного окисления ( ацетальдегида, формальдегида, уксусной кислоты и пр. В довольно редких случаях в отходящих газах содержится сажистый углерод.
Неполнота горения природного газа довольно часто наблюдалась в ряде отраслей промышленности при переводе на этот вид топлива печных и котельных агрегатов. Однако указанное можно объяснить пока еще несовершенством газогорелочных устройств, методов и режимов сжигания природного газа, и ни в коем случае нельзя делать вывод о том, что неполнота сжигания природного газа в различных технологических и энергетических установках присуща этому виду топлива. В равной степени это относится и к агрегатам цементной промышленности.
Факел горения природного газа находится вблизи устья го-релок. В результате сопло горелок перегревается и часто обгорает. Процесс обжига при этих горелках характеризуется работой печи на ближней зоне и повышенной температурой клинкера, поступающего в холодильник. Необходимо отметить, что, несмотря на завихрение газового потока и подачу первичного воздуха, смешение газа с вторичным воздухом при низких скоростях истечения газа из сопла горелки все же часто недостаточно полное, что проявляется в содержании в отходящих газах некоторого количества продуктов химического недожога природного газа.
Процесс горения природного газа является сложным и комплексным и определяется совместным действием кинетических, тепло-обменных и диффузионных процессов.
Расчет горения природного газа Елшанского месторождения вышеуказанного состава приведен в § 5 гл. В результате пересчета на сжигание природного газа с Коэффициентом избытка воздуха п 1 05 ( принимая к установке в печи инжек-ционные горелки) получим, что для сжигания 1 м3 газа при п 1 05 необходимо 9 79 м3 воздуха.
При горении природного газа развиваются высокие температуры, близкие к температурам горения мазута и необходимые условия плавления стали обеспечиваются при сжигании холодного природного газа с подогретым воздухом. Подогрев же природного газа для дальнейшего повышения температуры горения оказывается нерациональным ( стр.
Значительная температура горения природного газа обеспечивает возможность эффективного использования его для отопления высокотемпературных печей, где сжигание топлива других, низкосортных видов невозможно или связано со значительными трудностями и мало экономично.
Калориметрическая температура горения природного газа с избытком воздуха, соответствующим содержанию в продуктах горения 8 0 % — С02, 6 8 % — Оа и 85 2 % — N2 равна 1540 С ( см. табл. 81, стр.
Поскольку температура горения природного газа выше, чему низкокалорийных газов, следует примять меры против местного перегрева изделий и непосредственного омывания их факелом.
Поскольку температура горения природного газа выше, чем у низкокалорийных газов, следует принять меры против местного перегрева изделий и непосредственного омывания их факелом.
Теоретическая температура — горение
Теоретическая температура горения на выходе из топки для котлов, оборудованных различными газовыми горелками, при работе на природном газе составляет 1700 — 1900 С, что примерно на 300 — 600 С выше, чем при слоевом сжигании твердого топлива. Температура продуктов горения за котлом типа ДКВ при сжигании каменных углей по расчету составляет 310 — 320 С, а при сжигании природного газа 250 — 260 С. При испытании котла ДКВ-2, оборудованного вертикальными щелевыми горелками с нагрузкой 2 т / ч, получены температуры за котлом 170 — 175 С. При эксплуатационных испытаниях котлов типа ДКВ и ДКВР, оборудованных различными горелками, зафиксированы температуры продуктов горения за котлом от 230 до 270 С.
Теоретическая температура горения возрастает по мере приближения состава смеси к стехиометрическому и уменьшения содержания инертных компонентов, а также при увеличении начальной температуры смеси и др. При этом увеличивается взрывоопасность смеси; одновременно повышается и нормальная скорость горения. Таким образом, нормальная скорость горения может служить критерием взрывоопасное газовой смеси.
Теоретическая температура горения, подсчитанная с учетом диссоциации в условиях высокой температуры СОаиШО, равна 1950 при сжигании газа в стехиометрическом объеме сухого воздуха и при исходной температуре газа и воздуха — 0 С.
Теоретическая температура горения, подсчитанная с учетом диссоциации в условиях высокой температуры СОа и НаО, равна 1950, а с учетом содержания в воздухе 1 % влаги по весу — 1920 ( см. табл. 81, стр.
|
Зависимость энтальпии дымовых газов от коэффициента избытка воздуха и температуры дымовых газов ( топливо газообразное, Q 55400 кДж / кг.| Свойства газообразных топ лив. |
Теоретическая температура горения зависит от коэффициента избытка воздуха. При увеличении коэффициента избытка воздуха температура Та снижается.
Теоретическая температура горения возрастает по мере приближения состава смеси к стехиометрическому и уменьшения содержания инертных компонентов, а также при увеличении начальной температуры смеси и др. При этом увеличивается взрывоопасность смеси; одновременно повышается и нормальная скорость горения. Таким образом, величина нормальной скорости горения может служить критерием взрывоопасное газовой смеси.
Теоретическая температура горения, как видно из формулы (2.41), отличается от максимальной температуры только на значение теплоты диссоциации.
Теоретическая температура горения определяет пирометрический уровень в камере. Температура уходящих газов является реальной в выходном сечении камеры. В большинстве случаев она определяет наиболее низкий уровень температур в — камере. Поэтому логично ожидать, что величина эффективной температуры будет находиться между этими Двумя температурами и определять ее как функцию этих температур.
Теоретическая температура горения, как видно из формулы ( Х-3), отличается от жаропроизводительности только на величину теплоты диссоциации. Известно, что при высоких температурах в продуктах горения происходит диссоциация углекислоты и водяных паров.
Теоретическая температура горения ( / т) отличается от ка лориметрической тем, что учитывается понижение температуры за счет диссоциации продуктов горения.
|
Зависимость энтальпии дымовых газов от коэффициента избытка воздуха и температуры дымовых газов ( топливо газообразное, Qn 55400 кДж / кг.| Свойства газообразных топлив. |
Теоретическая температура горения зависит от коэффициента избытка воздуха. При увеличении коэффициента избытка воздуха температура Та снижается.
Теоретическая температура горения, полученная при условии полного сгорания топлива в теоретически необходимом для горения объеме воздуха, зависит от состава топлива и его теплоты сгорания. Так как процессы диссоциации практически могут идти при температурах горения свыше 1700 С, то теоретическая температура горения очень близка к калориметрической температуре.
Теоретическая температура горения определяется по значению тепловыделения в топке QR QE 26 732 кДж / кг с помощью 1 — Т табл. 6.6 Та 1707 К.